Kásler Miklós elmondta: 2017 nyarán törzskönyvezték a Spinraza nevű készítményt, amelyet 2018 elejétől Magyarországon is alkalmaznak az SMA-nak nevezett, gerincvelői eredetű izomsorvadás kezelésére. A kormányzat 2018-ban egymilliárd forint többletforrást biztosított a kezelésekre, és még abban az évben 30, azóta pedig további 24 gyermek kapta meg a kezelést.
A miniszter felhívta a figyelmet: a klinikai vizsgálatok eredményei igazolták a betegségcsoport további típusai esetében is a gyógyszer hatásosságát, ezért a kormányzat most további forrást biztosít rá.
A gyógyszer forgalmazójával született megállapodás szerint így minden, 18 év alatti gyermek hozzájuthat a jelenleg létező legkorszerűbb terápiához, vagyis
további 12-15 gyermek kezelése kezdődhet meg hamarosan, és minden eddigi terápiát is folytatni lehet.
Azok is részesülhetnek a kezelésben, akiknek a kérelmét eddig visszautasították.
Az érintettek a kedvező döntésekről szóló értesítéseket a jövő hét elején megkapják.
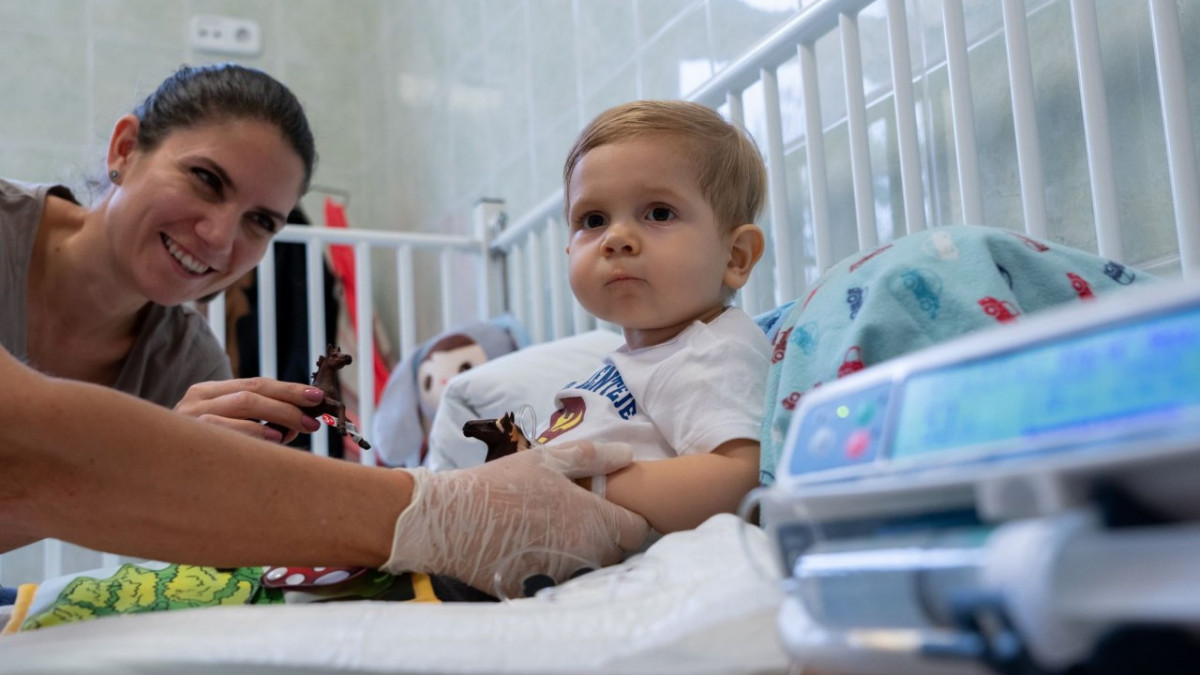
Kásler Miklós szólt arról is, hogy a terápiát két kisgyermeknél - Zenténél és Leventénél - nem alkalmazzák, az ő részükre ugyanis összegyűlt az Európában nem elérhető Zolgensma készítményre a forrás. A két kisgyermek terápiáját le kellett állítani ahhoz, hogy megkaphassák a génterápiát.
Mint mondta, a Zolgensma nevű készítményt nem törzskönyvezték Európában, csak az Egyesült Államokban. Hozzátette: a gyógyszer európai regisztrációja azért késik, mert kiderült, a cég az első fázisban végzett állatkísérletek eredményét manipulálta, ezért az amerikai hatóság a két évnél idősebbek esetében visszavonta a gyógyszer alkalmazási engedélyét. Megjegyezte: remélik, mielőbb tisztázódnak a körülmények, és ha az európai adminisztráció megadja az engedélyeket, Magyarország is dönt a kérdésben.
















































.jpg)